
De pH-waarde is één van meeteenheden waarmee we een voedingsproduct kunnen karakteriseren. Doorgaans wordt deze waarde als eenvoudig te meten eigenschap toegevoegd aan de lijst uit te voeren analyses. Maar vergis je niet: dat kan je duur komen te staan!
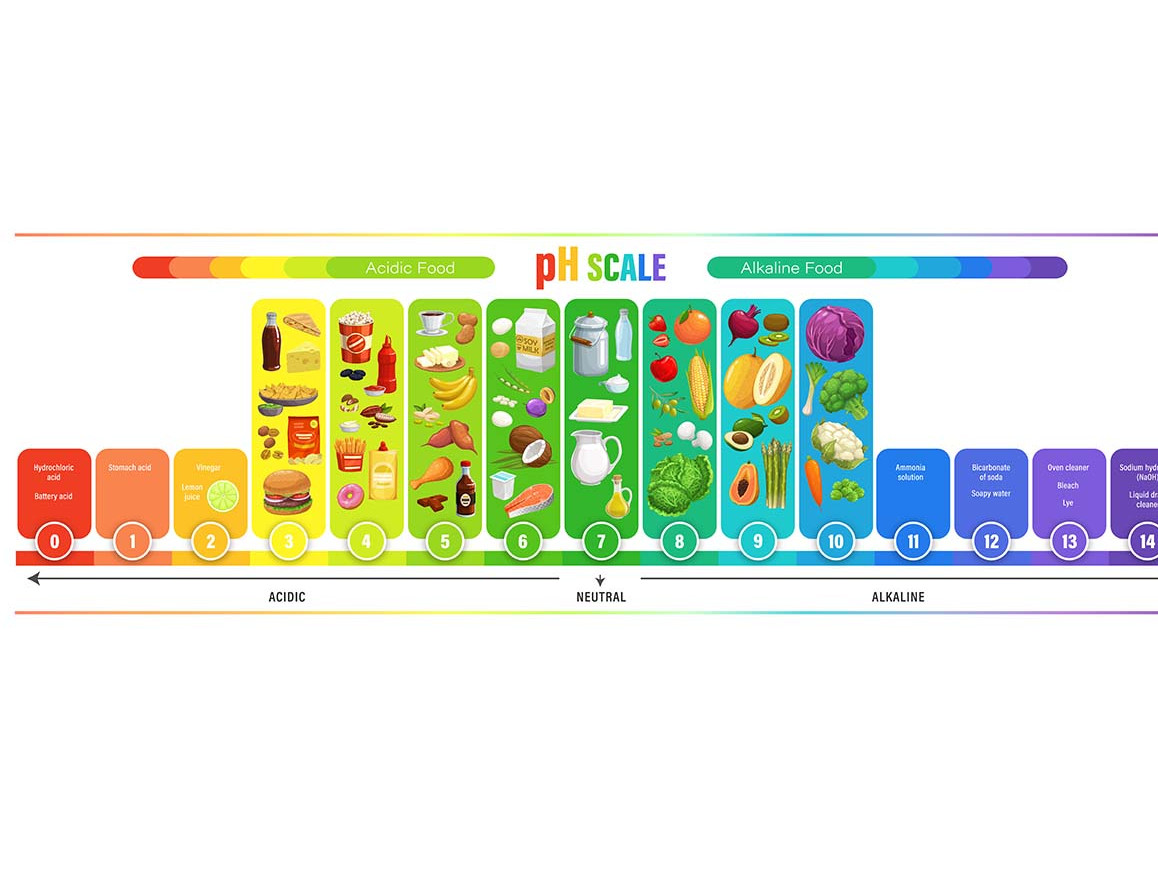
De pH is een maat voor de zuurtegraad van een waterige oplossing. Droge stoffen, poeders, puur vet en olie bevatten geen water; hierbij kan dan ook geen pH gemeten worden. Door het meten van de pH krijg je zicht op één of meer eigenschappen van het (eind)product; bijvoorbeeld de structuur, het vermogen tot schuimvorming, de houdbaarheid, kleur en/of smaak. De pH kan variëren van 0 tot 14, waarbij 1 sterk zuur is en 13 hoog alkalisch. Een neutrale oplossing heeft een pH van 7.
De pH wordt uitgedrukt als negatieve logaritme van de concentratie H3O+ ionen in die oplossing. In formulevorm is dit gedefinieerd als
Vaak wordt aangegeven dat pH de concentratie H+ is. Het juiste referentie-ion is het hydronium ion (H3O+), dat zich vormt als
Het meten van de pH kan met strips, een pH-indicator in de oplossing, of met een meetinstrument.
Het meten met een strip is gebasseerd op het feit dat de (chemische) verbinding lakmoes rood kleurt in een zure en blauw in een basische oplossing. De pH kan ook vastgesteld worden door een stukje lakmoespapier in de vloeistof te dompelen. De verkleurde strip wordt vergeleken met de bijgeleverde kleurenschaal.
Bij (chemische) processen is het vaak noodzakelijk de pH in de vloeistof te kennen, of wil je deze bijstellen naar een andere waarde. Dit kan door een pH-indicatorvloeistof toe te voegen die binnen een nauwe pH-range van kleur verandert. Deze pH-indicatoren zijn echter niet food grade.
Meetinstrumenten om de pH te meten werken allemaal volgens hetzelfde meetprincipe: een sensor (electrode) die gevoelig is voor het waterstof-ion stelt de concentratie hydronium-ionen vast en vergelijkt deze met een referentiesignaal. De meet-electrode geeft een potentiaal op basis van de aanwezige waterstofionen, de referentie electrode geeft een vast potentiaal. Het potentiaalverschil tussen deze twee is een maat voor de pH van de oplossing.
Goed om te weten is dat de factor temperatuur het potentiaalverschil tussen beide electrodes beïnvloedt. Bij een lage temperatuur neemt de spanning af, bij een hogere temperatuur neemt deze toe. Voor nauwkeurige metingen moet je hiervoor compenseren. Moderne pH-sensoren beschikken doorgaans over een zogenaamde Automatische Temperatuur Compensatie (ATC).
Er zijn verschillende typen pH-sensoren. Zo zijn er sensoren met een puntvormige tip om in ‘vaste stoffen’ te meten en sensoren waarbij er een mes voor de tip is geplaatst zodat bijvoorbeeld vlees eerst kan worden ingesneden.
Vervuiling op de sensor kan de meting flink verstoren. pH-meters geven ondanks vervuiling wel een waarde aan. Het is goed om je te realiseren dat deze waarde veelal niet correct is. Reinigen van de electrode mag alleen gebeuren met een speciale reinigingsvloeistof. Dit om te voorkomen dat de gevoelige membraan beschadigt.
Kalibreren van de pH-meter doe je met buffer-oplossingen. Vaak is een tweepunts kalibratie voldoende. Dan kan je volstaan met een bufferoplossing in het zure traject (pH 4) en in het neutrale traject (pH 7). Soms wordt een driepuntskalibratie uitgevoerd, waarbij een meting in een alkalische buffer (pH 10) wordt toegevoegd. Kalibratie moet minimaal elke dag (voorafgaand aan de meting) worden uitgevoerd.
Het meten van de pH moet op de juiste manier gebeuren. De gebruikte werkwijze en methode moet duidelijk worden gerapporteerd. Alleen op die manier kunnen de gegevens juist worden geïnterpreteerd en kan de meting door anderen worden herhaald.
Referentie:
https://nl.wikipedia.org/wiki/Lakmoes
https://nl.wikipedia.org/wiki/PH-indicator
pH theory guide Mettler Toledo
Hanna Instruments, wat is pH
Bron: Vakblad Voedingsindustrie april 2024